- DNA tự do là gì ?
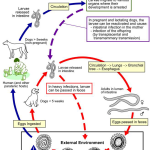
DNA tự do (cell-free DNA – cfDNA) được giải phóng từ các tế bào vào hệ thống tuần hoàn và di chuyển khắp cơ thể. Trong một số điều kiện sinh lý hoặc bệnh lý, chẳng hạn như mang thai, cấy ghép nội tạng và ung thư, các mô liên quan bị ảnh hưởng có thể giải phóng DNA vào hệ thống tuần hoàn ngoại vi. Do đó, việc phát hiện cfDNA trong máu ngoại vi có thể xác định những bất thường của các bệnh nhân theo cách không xâm lấn. Trong những năm gần đây, nhiều công nghệ đã xuất hiện dựa trên phân tích cfDND cho xét nghiệm tiền sản không xâm lấn (NIPT), theo dõi cấy ghép nội tạng và phát hiện các bệnh miễn dịch cũng như ung thư. Trong giải phẫu bệnh học, nhiều nghiên cứu về dấu ấn sinh học dựa trên phân tích các mô khối u thu được từ các thủ thuật phẫu thuật xâm lấn có thể gặp khó khăn trong việc sinh thiết ở một số trường hợp, vì vậy, việc phát triển các phương pháp mới không xâm lấn là rất cần thiết. Phân tích cfDNA đã thu hút sự chú ý ngày càng tăng vì khả năng tiếp cận dễ dàng, tính chất không xâm lấn và tính đặc hiệu của khối u tiềm năng thông qua phát hiện bằng các phương pháp ứng dụng sinh học phân tử hiện đại như Real-time PCR định lượng hoặc giải trình tự đặc hiệu. Các phương pháp phân tích dựa trên cfDNA được sử dụng rộng rãi trong nhiều lĩnh vực chẩn đoán và tiên lượng ung thư, cũng như kháng thuốc ung thư và sàng lọc sớm.
Hình 1: DNA tự do lưu chuyển trong hệ tuần hoàn
- Ý nghĩa của cfDNA trong phát hiện đột biến kháng thuốc trên gen EGFR ở bệnh nhân ung thư phổi không tế bào nhỏ (NSCLC)
Trong những năm gần đây, cfDNA đã nổi lên như một dấu ấn sinh học dựa trên huyết tương có độ nhạy và đặc hiệu tốt để phát hiện các đột biến trên gen EGFR gây kháng thuốc điều trị ở bệnh nhân NSCLC. Trong các dạng đột biến EGFR, T790M là đột biến tạo nên cơ chế kháng các thuốc ức chế hoạt tính tyrosine kinase của EGFR (EGFR-TKI) phổ biến nhất, có thể phát hiện được trong gần 60% mẫu sinh thiết mô được thực hiện sau khi quá trình kháng thuốc khởi phát ở bệnh nhân đang được điều trị. Một số nghiên cứu đã chứng minh rằng các đột biến, bao gồm T790M, được phát hiện trong cfDNA thu nhận từ huyết tương có độ tương đồng cao với các đột biến được phát hiện trong mô khối u ở cùng một bệnh nhân. Như vậy, kết quả của những nghiên cứu vừa đề cập chỉ ra rằng phát hiện sự hiện diện cfDNA có trong bệnh phẩm sinh thiết mô lỏng là một phương pháp thay thế khả thi và giảm tối thiểu tổn thương xâm lấn so với sinh thiết mô rắn. Các ứng dụng lâm sàng khác của cfDNA trong lĩnh vực này bao gồm chẩn đoán mức độ phân tử cho bệnh, theo dõi liên tục quá trình đáp ứng thuốc bệnh nhân theo thời gian thực để kịp thời phát hiện sự phát sinh các đột biến kháng thuốc (điều này gần như không thể thực hiện được với sinh thiết mẫu mô rắn nhiều lần lặp lại), quản lý lâm sàng bệnh nhân. Một điểm đáng lưu ý khác là do phân tích cfDNA không liên quan đến quá trình cố định formaldehyde nên tần suất kết quả dương tính giả do khử amin sẽ giảm xuống.
- Xét nghiệm Allele-specific PCR (ASPCR) phát hiện đột biến kháng thuốc trên gen EGFR
ASPCR là một dạng ứng dụng PCR cho phép phát hiện trực tiếp bất kỳ đột biến điểm nào trong DNA người với quy trình đơn giản, giá thành thấp hơn so với các phương pháp giải trình tự. Nguyên tắc của phương pháp ASPCR dựa trên việc mồi oligonucleotide tạo thành điểm không khớp ở đầu 3′- OH với bản mẫu DNA sẽ gây khó khăn cho sự hoạt động của Taq DNA polymerase. Do đó, chỉ các mồi oligonucleotide đặc hiệu cho tất cả các allele đột biến được kéo dài để tạo mạch mới trong khi các allele hoang dại sẽ không được nhân bản.
Mẫu cfDNA sau khi được tách chiết sẽ được phát hiện đột biến EGFR trong mẫu cfDNA sử dụng 7 cặp mồi xác định trình tự cặp base đặc hiệu cho mỗi dạng đột biến đích và 1 cặp mồi được thiết kế để phát hiện dạng hoang dại của exon 28 của gen EGFR sử dụng làm chứng nội cho toàn bộ quy trình. Kết quả sẽ được phân tích theo bảng sau:
| Phản ứng | Loại đột biến EGFR được phát hiện | Exon | Kênh màu huỳnh quang |
| 1 | Mất đoạn Exon 19 | 19 | FAM |
| S768I | 20 | JA270 | |
| IC (WT exon 28) | 28 | Cy 5.5 | |
| 2 | L858R | 21 | FAM |
| T790M | 20 | JA270 | |
| IC (exon 28 hoang dại) | 28 | Cy 5.5 | |
| 3 | L861Q | 21 | FAM |
| G719X | 18 | HEX | |
| Thêm đoạn Exon 20 | 20 | JA270 | |
| IC (exon 28 hoang dại) | 28 | Cy 5.5 |
Nếu mẫu bệnh nhân cho kết quả dương tính tương ứng với kênh màu nào trong bảng chứng tỏ có sự xuất hiện đột biến trong gen EGFR, từ đó, bác sĩ có thể đưa ra khuyến cáo hướng điều trị phù hợp với từng tình trạng đột biến của bệnh nhân.
ThS. Quốc Kỳ Duyên – Khoa KTXNYH (Tổng hợp)
TÀI LIỆU THAM KHẢO
- M. Cisneros-Villanueva, L. Hidalgo-Pérez, M. Rios-Romero et al. Cell-free DNA analysis in current cancer clinical trials: a review. Br J Cancer 126, 391–400 (2022).
- J.Y. Douillard, G. Ostoros, M. Cobo, T. Ciuleanu, R. Cole, G. McWalter, et al. Gefitinib treatment in EGFR mutated caucasian NSCLC: circulating-free tumor DNA as a surrogate for determination of EGFR status J. Thorac. Oncol., 9 (2014), pp. 1345-1353
- J.Y. Douillard, G. Ostoros, M. Cobo, T. Ciuleanu, R. McCormack, A. Webster, et al.
First-line gefitinib in Caucasian EGFR mutation-positive NSCLC patients: a phase-IV, open-label, single-arm study Br. J. Cancer, 110 (2014), pp. 55-62
- E.A. Punnoose, S. Atwal, W. Liu, R. Raja, B.M. Fine, B.G. Hughes, et al. Evaluation of circulating tumor cells and circulating tumor DNA in non-small cell lung cancer: association with clinical endpoints in a phase II clinical trial of pertuzumab and erlotinib Clin. Cancer Res., 18 (2012), pp. 2391-2401
- L. Ugozzoli, R. Bruce Wallace. Allele-specific polymerase chain reaction. Methods Vol. 2, Issue 1, Pages 42-48 (1991).
- cobas® EGFR mutation test v2 Instruction for Use (Roche Diagnostic GMBH).
 1900 2039
1900 2039