NTTU – Phát hiện sớm đa loại ung thư thông qua sinh thiết lỏng
Ung thư hiện là nguyên nhân gây tử vong sớm đứng thứ hai trên toàn cầu, chủ yếu do phần lớn các ca được phát hiện ở giai đoạn muộn. Các phương pháp sàng lọc ung thư hiện nay còn hạn chế, thường chỉ phát hiện được một số ít loại ung thư, với giá trị dự đoán dương tính thấp và mức độ tuân thủ của bệnh nhân chưa tối ưu. Trong những năm gần đây, xét nghiệm sinh thiết lỏng trong phát hiện sớm đa ung thư (MCED – Multi-Cancer Early Detection) đã nổi lên như một hướng tiếp cận đầy hứa hẹn nhằm cách mạng hóa công tác kiểm soát ung thư.
Sự phát triển của các công nghệ MCED
Quá trình phát triển của xét nghiệm phát hiện sớm đa ung thư dựa trên sinh thiết lỏng đã trải qua hai giai đoạn quan trọng:
Giai đoạn đầu: xác định một dấu ấn khối u đơn lẻ có khả năng phát hiện đồng thời nhiều loại ung thư. Các dấu ấn sinh học dựa trên protein như Carcinoembryonic Antigen (CEA) và Carbohydrate Antigen 15-3 (CA15-3) là những dấu ấn đầu tiên được nghiên cứu. Tuy nhiên, các dấu ấn này chỉ phát hiện được một số loại ung thư giới hạn, ví dụ CEA chủ yếu liên quan đến ung thư phổi, đại trực tràng, dạ dày và tụy. Bên cạnh đó, các biomarker này có độ nhạy thấp và không thể xác định chính xác mô khởi phát ung thư (TOO – tissue of origin), làm hạn chế đáng kể việc ứng dụng rộng rãi trong sàng lọc đa ung thư.
Giai đoạn thứ hai: bắt đầu với sự ra đời của các công nghệ giải trình tự thế hệ mới (NGS – Next Generation Sequencing), giúp việc phân tích hệ gen quy mô lớn. Trọng tâm nghiên cứu chuyển sang phát hiện DNA khối u lưu hành (ctDNA) và các biến đổi di truyền khác, sinh thiết lỏng dựa trên ctDNA có thể chẩn đoán đồng thời nhiều loại ung thư và xác định nguồn gốc của tín hiệu ung thư.
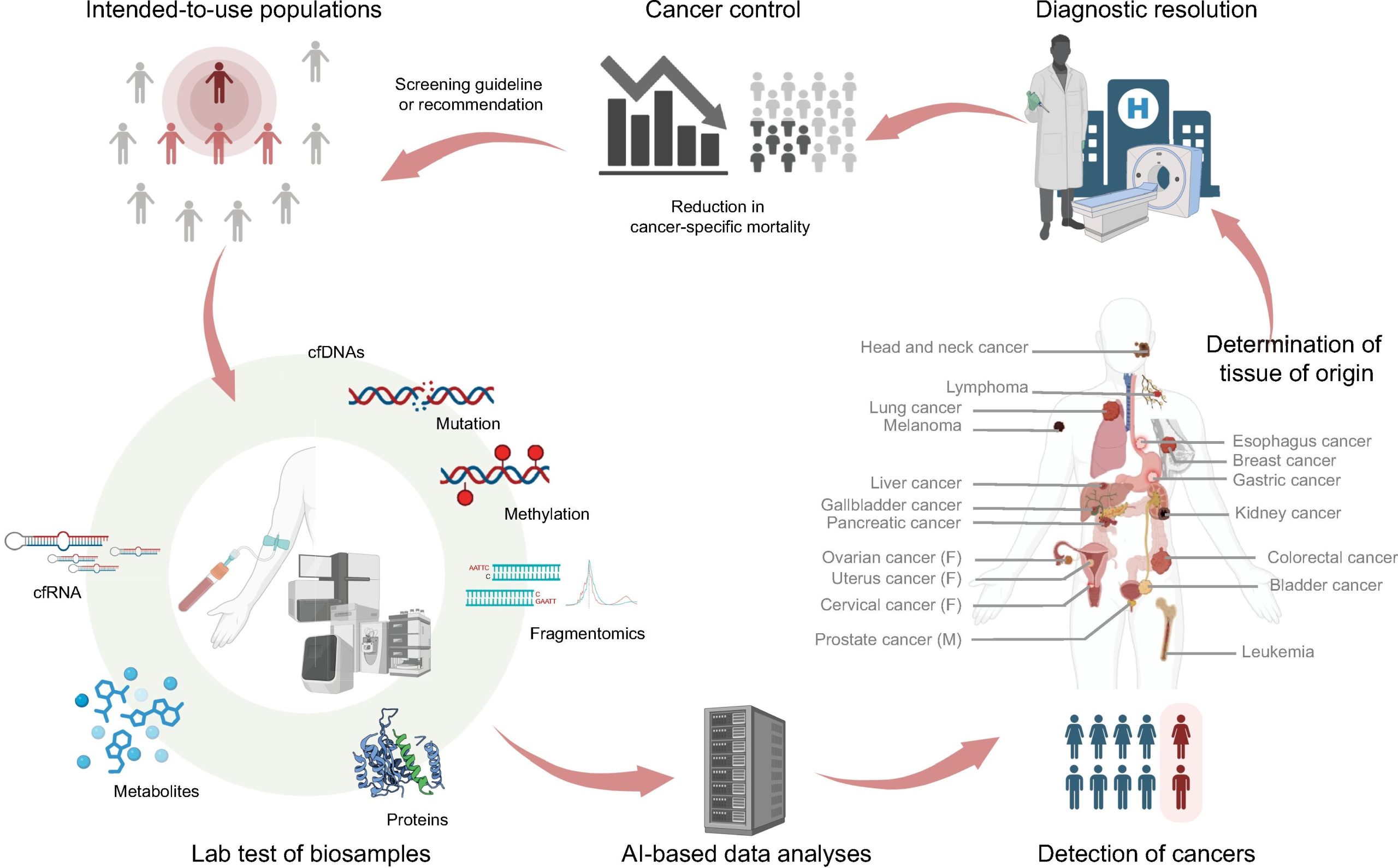
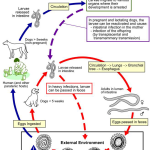
Mẫu và dấu ấn sinh học trong MCED
Sinh thiết lỏng có thể được thực hiện trên nhiều loại mẫu sinh học khác nhau, bao gồm:
- Máu (huyết tương, huyết thanh, máu toàn phần, hồng cầu)
- Nước tiểu
- Nước bọt
- Dịch não tủy (CSF) và các dịch sinh học khác.
Trong đó, máu – đặc biệt là huyết tương – được sử dụng phổ biến nhất nhờ tính không xâm lấn, quy trình thu mẫu tiêu chuẩn hóa và tính khả thi cao trong lâm sàng.
Các dấu ấn sinh học từ máu phục vụ cho MCED bao gồm:
- cfDNA (cell-free DNA)
- cfRNA (cell-free RNA)
- Protein lưu hành
- Chất chuyển hóa lưu hành
- Các phân tử sinh học khác
Chuyển hóa chất tuần hoàn
Dấu ấn chuyển hóa của khối u được định nghĩa là các chất chuyển hóa có trong máu hoặc các dịch cơ thể khác, cung cấp thông tin quan trọng về trạng thái chuyển hóa và đặc điểm sinh học của tế bào ung thư. Ung thư về bản chất là một bệnh lý chuyển hóa, và sự khởi phát ung thư luôn đi kèm với rối loạn trong các con đường chuyển hóa.
Bộ chuyển hóa là một thực thể toàn diện, mang lại cái nhìn tổng thể về toàn bộ quá trình chuyển hóa tế bào, có vai trò như biểu hiện kiểu hình trực tiếp nhất, phản ánh một cách khách quan xu hướng thay đổi tổng thể xảy ra ở mức DNA, RNA và protein trong tế bào, phát hiện sớm một số loại ung thư riêng lẻ, chẳng hạn như ung thư tụy, ung thư dạ dày và ung thư tuyến tiền liệt.
Ứng dụng trí tuệ nhân tạo trong MCED
các dấu ấn sinh học đơn lẻ thường không đáp ứng đủ yêu cầu của chẩn đoán sớm ung thư. Để nâng cao hiệu quả của kỹ thuật sinh thiết lỏng, cần ứng dụng phân tích toàn diện các bộ dữ liệu dựa trên hệ gen học, phiên mã học, biểu sinh học toàn hệ gen và khối phổ. Các bộ dữ liệu này khác biệt đáng kể so với dữ liệu xét nghiệm truyền thống, vì chúng có định dạng phức tạp hơn, quy mô lớn hơn, độ chiều dữ liệu cao hơn và nhiễu nhiều hơn. Do đó, MCED đòi hỏi sự tích hợp của trí tuệ nhân tạo (AI) cùng các thuật toán học máy tiên tiến nhằm hỗ trợ phân tích toàn diện các bộ dữ liệu quy mô lớn.
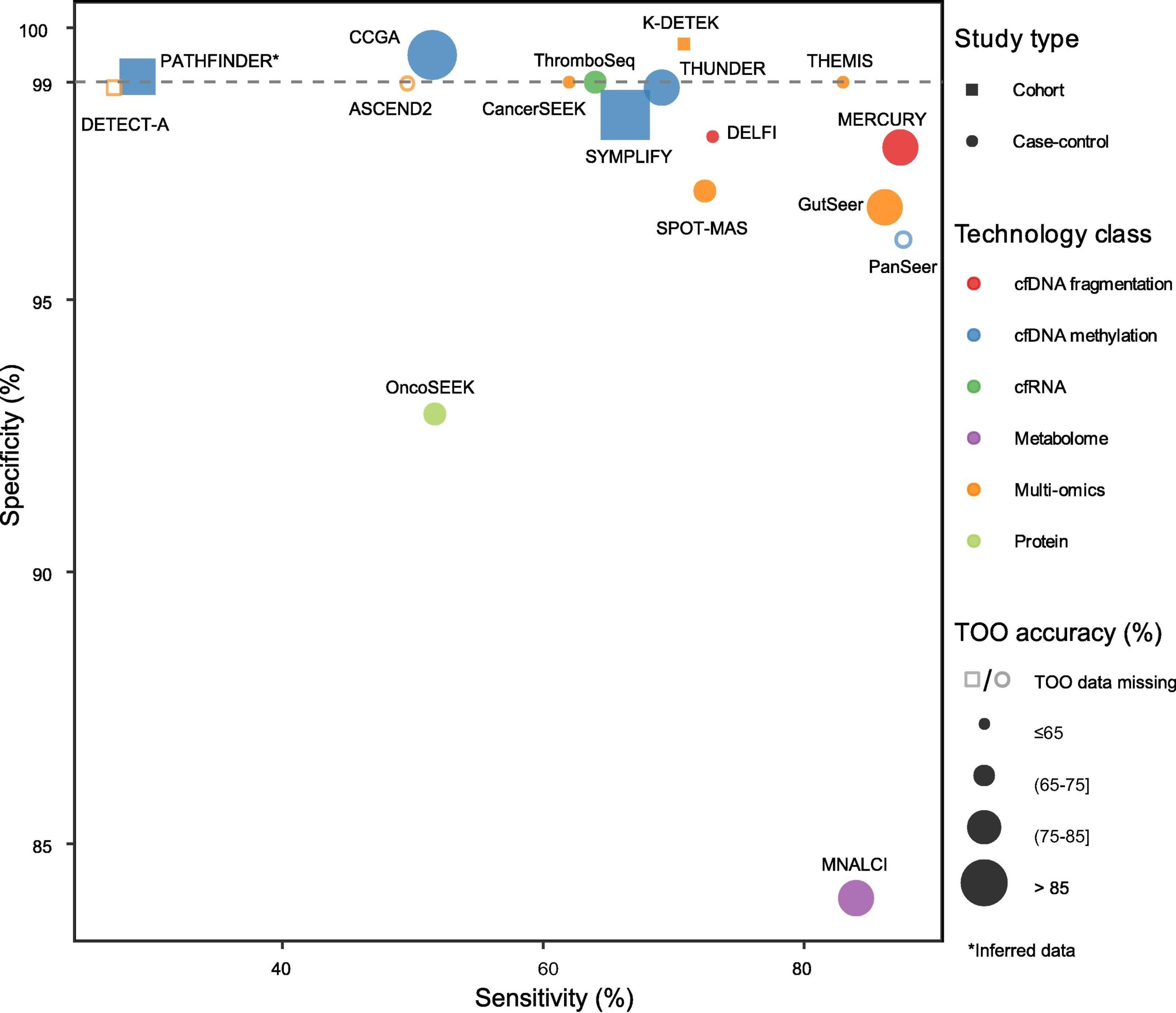
Hiệu năng của các công nghệ MCED
Một trong những đặc điểm kỹ thuật nổi bật của MCED là độ đặc hiệu rất cao, đặc biệt khi sử dụng các phương pháp dựa trên cfDNA. Độ đặc hiệu MCED dao động từ 84% đến 99,7%. Đây là một ưu thế đáng kể, bởi MCED được thiết kế để ứng dụng trên quy mô lớn trong quần thể người không có triệu chứng. Độ đặc hiệu cao đóng vai trò quan trọng trong việc giảm thiểu số lượng ca dương tính giả trong nhóm đối tượng này.
Trong khi duy trì độ đặc hiệu cao, MCED lại cho thấy độ nhạy (sensitivity) thay đổi tùy theo nhóm dấu ấn sinh học, cụ thể:
- cfDNA methylation: 28,9% – 87,6%
- cfDNA fragmentomics: 73% – 87,4%
- cfRNA: 64%
- Protein: 51,7%
- Multi-omics: 27,1% – 86,2%.
Các phân tích so sánh cho thấy MCED có giá trị tiên đoán dương tính (PPV – Positive Predictive Value) vượt trội hơn so với các phương pháp sàng lọc truyền thống. Trong nghiên cứu PATHFINDER, MCED đạt PPV = 38%, trong khi các phương pháp sàng lọc thường quy có PPV thấp hơn nhiều, như:
- Chụp nhũ ảnh (mammography) trong sàng lọc ung thư vú: 6–7%
- Xét nghiệm HPV trong sàng lọc loạn sản cổ tử cung mức CIN3+: 7,2%
- Chụp CT liều thấp (LDCT) trong sàng lọc ung thư phổi: 4%
Một đặc điểm quan trọng khác của MCED là khả năng xác định vị trí khối u (TOO – Tissue of Origin) của các ca ung thư được phát hiện yếu tố cần thiết cho việc ứng dụng hiệu quả MCED trong sàng lọc quần thể không triệu chứng.
MCED có thể giảm thiểu việc thực hiện các thủ thuật hình ảnh và sinh thiết không cần thiết. Cách tiếp cận có mục tiêu này không chỉ giúp chẩn đoán kịp thời và chính xác hơn, mà còn giảm bớt lo âu và căng thẳng cho cả bệnh nhân và bác sĩ. MCED cho thấy tỷ lệ xác định đúng vị trí mô ung thư khá cao, dao động từ 52,9% đến 88,7%. Đáng chú ý, những nghiên cứu ứng dụng đặc trưng methyl hóa thường đạt độ chính xác xác định vị trí cao hơn rõ rệt so với các nghiên cứu chỉ dựa trên các chỉ dấu khác.
Đánh giá MCED trong giai đoạn phát triển lâm sàng và khuyến nghị
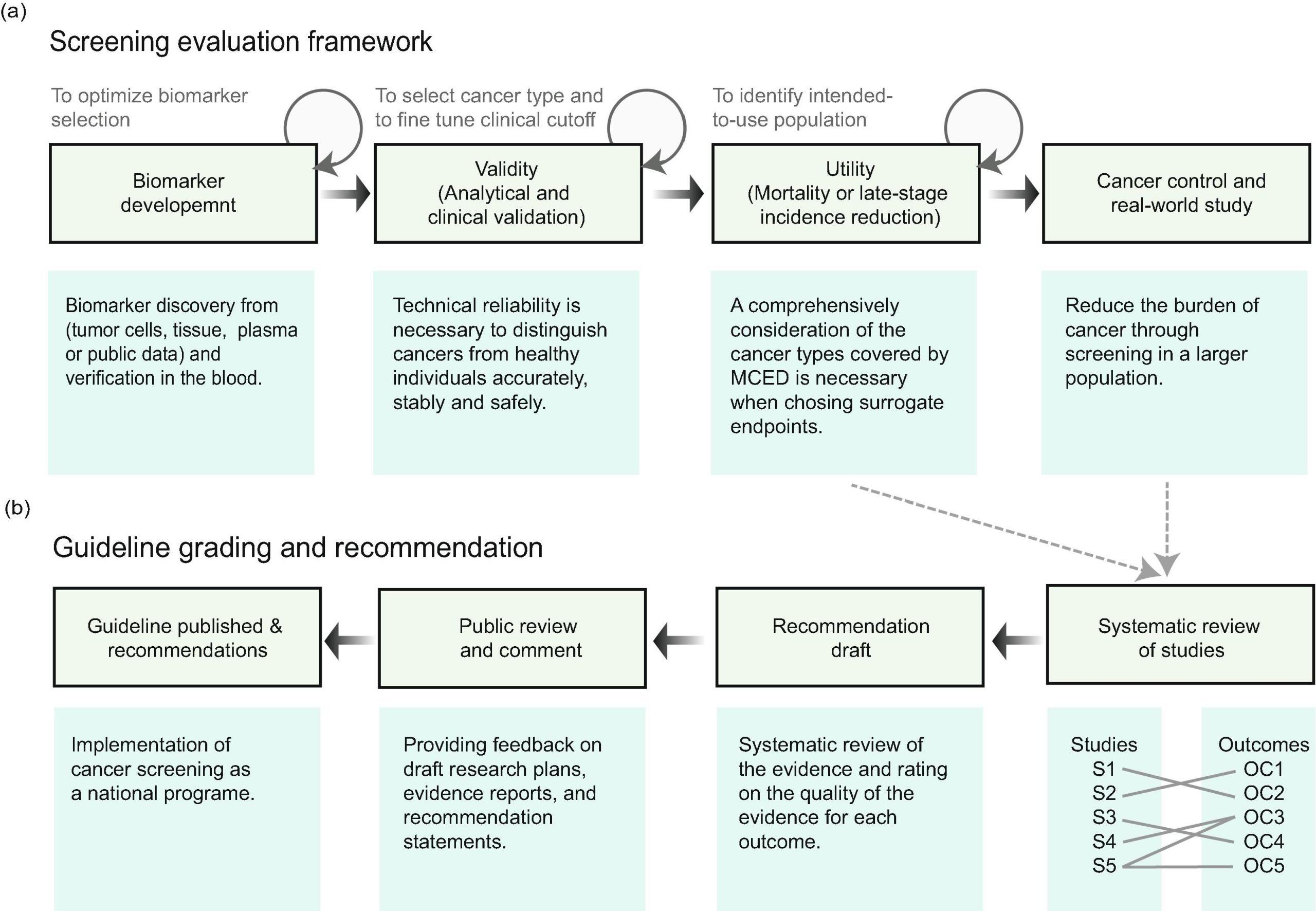
(a) Nhiều yếu tố được xem xét trong khung đánh giá MCED, bao gồm:
- Phát hiện dấu ấn sinh học (biomarker discovery)
- Đánh giá hiệu năng phân tích và hiệu quả lâm sàng (analytical and clinical efficacy studies),
- Đánh giá giá trị ứng dụng lâm sàng (clinical utility evaluations),
- Và nghiên cứu thực tế (real-world studies).
(b) Nếu xét nghiệm MCED được các cơ quan quản lý phê duyệt, bước tiếp theo là xây dựng khuyến nghị và phân loại hướng dẫn (guideline recommendation and grading) nhằm triển khai và mở rộng việc sàng lọc MCED ra cộng đồng dân số rộng hơn.
Các bước quan trọng trong quy trình này bao gồm:
- Tổng quan hệ thống (systematic review) và đánh giá chất lượng các thử nghiệm lâm sàng hiện có,
- Soạn thảo đề cương khuyến nghị ban đầu,
- Lấy ý kiến công khai và tích hợp phản hồi từ cộng đồng chuyên môn,
- Chỉnh sửa và hoàn thiện bản dự thảo,
- Cuối cùng, công bố chính thức khuyến nghị và hướng dẫn lâm sàng.
Cải thiện độ nhạy trong thực hành
Hạn chế nổi bật nhất của các xét nghiệm MCED hiện nay nằm ở độ nhạy còn tương đối thấp. Nguyên nhân của hạn chế này chủ yếu đến từ hai yếu tố chính: kỹ thuật và lâm sàng.
Về khía cạnh kỹ thuật, độ nhạy phân tích còn hạn chế, đặc biệt là giới hạn phát hiện (LoD) quá thấp, có thể dẫn đến không phát hiện được các chất phân tích có nguồn gốc từ khối u ở nồng độ rất thấp. Một số loại ung thư như ung thư vú, ung thư đường tiết niệu và ung thư tuyến tiền liệt có xu hướng giải phóng rất ít DNA khối u lưu hành (ctDNA) vào máu. Do đó, khả năng phát hiện những loại ung thư này bằng MCED thấp hơn. Bên cạnh đó, việc phát hiện các sản phẩm có nguồn gốc từ khối u ở giai đoạn sớm hoặc trong tổn thương tiền ung thư như u tuyến đại tràng tiến triển, loạn sản biểu mô cổ tử cung (CIN), hay loạn sản biểu mô mức độ cao ở dạ dày vẫn là một thách thức lớn.
Ngoài ra, tính dị thể của ung thư có thể dẫn đến sự không chính xác trong phân loại từng loại ung thư, làm giảm hiệu quả của bộ phân loại. Những hạn chế này là mối quan ngại đáng kể, vì chúng ảnh hưởng trực tiếp đến khả năng phát hiện sớm và độ tin cậy của xét nghiệm MCED.
Kết luận
Sự phát triển của các công nghệ sinh thiết lỏng đã mở đường cho sự ra đời của MCED phương pháp sàng lọc ung thư dựa trên các dấu ấn sinh học lưu hành trong máu, mang lại tiềm năng đột phá trong lĩnh vực sàng lọc ung thư. Với hiệu năng vượt trội, bao gồm độ đặc hiệu cao, giá trị tiên đoán dương tính thuận lợi và khả năng xác định chính xác vị trí khối u, MCED được kỳ vọng sẽ tối ưu hóa các mô hình sàng lọc hiện nay và giảm tỷ lệ tử vong do ung thư. Khi bước vào kỷ nguyên mới của sàng lọc ung thư, MCED có thể mang tính cách mạng trong phát hiện sớm, giúp cải thiện tiên lượng và chất lượng cuộc sống của bệnh nhân trên toàn cầu.
TÀI LIỆU THAM KHẢO
- Yongjie Xu, Sibo Zhu, Changfa Xia, Hui Yu, Si Shi, Kezhong Chen, et al. Liquid biopsy-based multi-cancer early detection: an exploration road from evidence to implementation. Science Bulletin. 2025.
- Nguyen Luu Hong Dang, Nguyen Thi Hue Hanh, Le Van Hoi, Bui Vinh Quang, Nguyen Lan Hieu, Pham Nhu Hiep, et al. Prospective validation study: a non-invasive circulating tumor DNA-based assay for simultaneous early detection of multiple cancers in asymptomatic adults. BMC medicine. 2025;23(1):90.
- Ignaty Leshchiner, Edmund A Mroz, Justin Cha, Daniel Rosebrock, Oliver Spiro, Juliana Bonilla-Velez, et al. Inferring early genetic progression in cancers with unobtainable premalignant disease. Nature cancer. 2023;4(4):550-63.
Nguyễn Thị Nhạn – KTXNYH
 1900 2039
1900 2039